外源褪黑素对产蛋后期蛋鸡生产性能、血清指标及体内褪黑素含量的影响
郝二英,黄晨轩,孙浩政,王德贺,周荣艳,黄仁录,陈辉
摘要:为了研究不同浓度的外源褪黑素对产蛋后期蛋鸡生产性能、体内褪黑素含量及血清指标的影响,本试验随机选取健康、体重相近的70周龄大午金凤蛋鸡60只,随机分为3组,每组4个重复,每个重复5只。对照组腹腔注射等量生理盐水,试验Ⅰ组腹腔注射褪黑素20 mg/(kg·d),试验Ⅱ组腹腔注射褪黑素50 mg/(kg·d)。光照条件为16L∶8D,预试期7 d,正试期28 d。结果显示:1)与对照组相比,褪黑素处理极显著提高了第15~21天和第22~28天蛋鸡的产蛋率(P< 0.01),显著提高了大白卵泡的数量(P< 0.05),但并没有对蛋品质造成显著的影响(P>0.05)。2)与对照组相比,在第21和28天时,褪黑素处理显著或极显著提高了血清和蛋黄中的褪黑素含量(P< 0.05或P< 0.01);在第28天时,50 mg/(kg·d)褪黑素极显著提高了卵巢中的褪黑素含量(P< 0.01)。3)与对照组相比,在第21和28天时,50 mg/(kg·d)褪黑素极显著提高了血清和蛋黄中超氧化物歧化酶(SOD)活性及总抗氧化能力(T-AOC)(P< 0.01),极显著降低了氧自由基(ROS)含量(P< 0.01);在第28天时,50 mg/(kg·d)褪黑素极显著提高了卵巢中SOD活性及T-AOC(P< 0.01),极显著降低了ROS含量(P< 0.01)。4)与对照组相比,在第21和28天时,50 mg/(kg·d)褪黑素极显著提高了血清免疫球蛋白(Ig)A、IgG、IgM含量(P< 0.01)。5)与对照组相比,在第21和28天时,褪黑素处理极显著提高了血清促卵泡激素(FSH)和促黄体素(LH)含量(P< 0.01)。综上,外源褪黑素显著提高了产蛋后期蛋鸡的产蛋率,提高了机体的抗氧化性能、免疫性能及生殖激素水平,为产蛋后期外源补充褪黑素提高产蛋性能提供理论依据。
关键词:褪黑素;产蛋后期;产蛋率;抗氧化指标;卵泡数量
Effects of Exogenous Melatonin on Performance, Serum Indexes and Melatonin Content of Laying Hens during Later Laying Period
HAO Erying , HUANG Chenxuan , SUN Haozheng , WANG Dehe , ZHOU Rongyan , HUANG Renlu , CHEN Hui
Abstract: To investigate the effects of different concentrations of exogenous melatonin on performance, melatonin content and serum indexes of laying hens during later laying period, 60 healthy Dawu Jinfenglaying hens with similar healthy body weight were randomly divided into 3 groups, each group had 4 repetitions, and each had 5 repetitions. The control group was intraperitoneally injected normal saline. The test group Ⅰ was injected intraperitoneally with 20 mg/(kg·d) melatonin, and the test group Ⅱ was intraperitoneally injected with 50 mg/(kg·d) melatonin. The illumination condition was 16L: 8D, the test period included a 7-d pre-test period and a 28-d trial period. The results showed as follows: 1) compared with the control group, the melatonin treatment significantly increased the laying rate at d 15 to 21 and d 22 to 28 (P< 0.01), and significantly increased the number of large white follicles (P< 0.05), but had no significant effect on egg quality (P>0.05). 2) Compared with the control group, the melatonin treatment significantly increased the melatonin contents in the serum and yolk at d 21 and 28 (P< 0.05 or P< 0.01); at d 28, the 50 mg/(kg·d) melatonin treatment significantly increased the melatonin contnet in the ovaries (P< 0.01). 3) Compared with the control group, at d 21 and 28, 50 mg/(kg·d) melatonin significantly increased the superoxide dismutase (SOD) activity and total antioxidant capacity (T-AOC) (P< 0.01), and significantly reduced the content of oxygen free radicals (ROS) (P< 0.01); at d 28, 50 mg/(kg·d) melatonin significantly increased the activity of SOD and T-AOC (P< 0.01), and significantly reduced the content of ROS in the ovary (P< 0.01). 4) Compared with the control group, at d 21 and 28, 50 mg/(kg·d) melatonin significantly increased the serum immunoglobulin (Ig) A, IgG and IgM contents (P< 0.01). 5) Compared with the control group, melatonin treatment significantly increased the follicle-stimulating hormone (FSH) and luteotropin (LH) contents in serum at d 21 and 28 (P< 0.01). Exogenous melatonin treatment significantly improves the laying rate of laying hens in the later laying period, improves the body's antioxidant performance, immune performance, and reproductive hormone levels. It provided a theoretical basis for exogenous melatonin supplementation to improve egg production during the end of laying.
Key words:melatoninlater laying periodlaying rateantioxidant indexnumber of follicles
如何延长蛋鸡产蛋期,实现“100周龄500只蛋”是近年来国外育种公司的热点研究之一。众所周知,在蛋鸡产蛋后期,蛋鸡的产蛋性能降低[1-2]、蛋品质下降、破蛋率增加[3]、平均产蛋间隔增加[4]、卵巢上的卵泡数目减少、闭锁卵泡数目增加[5]。然而,在产蛋后期,卵巢加速老化的机制尚不完全清楚。因此,延缓卵巢衰老和预防卵巢功能障碍是家禽生产中首要解决的问题。褪黑素(N-乙酰基-5-甲氧基色胺)在20世纪50年代首次在松果腺中发现[6],是由松果体分泌的一种吲哚类的神经内分泌激素,其生物学作用十分广泛。褪黑素是协调光照信息与生殖系统关系的重要激素,作用于下丘脑-垂体-性腺轴中的多个位点,从而参与对动物生殖、内分泌、免疫和神经系统的生物调节[7-8],还有维持昼夜节律、改善睡眠、镇静镇痛、抗应激、抗衰老、抗氧化、抗肿瘤和增强机体的免疫力等诸多功能[9-11]。已有研究发现,血液中褪黑激素含量与鸡的年龄呈反比,在产蛋后期褪黑素含量显著降低[12]。产蛋后期蛋鸡产蛋率急剧下降,但是研究发现体内仍然有大量发育的卵泡。如果从生理学的角度出发,通过生理调节如外源注射褪黑素促进卵泡的生长发育,降低卵泡的闭锁率,从而提高产蛋后期的产蛋率是否可行?而且以前的褪黑激素研究主要集中在其对产蛋高峰期或家禽早期的影响,因此,本研究拟探讨褪黑激素对产蛋后期蛋鸡的影响,研究外源褪黑素处理是否可以延缓蛋鸡卵巢衰老,是否可以提高蛋鸡的产蛋率,以期为褪黑素在家禽生产中的应用提供理论依据。

1 材料与方法
1.1试验动物及饲粮
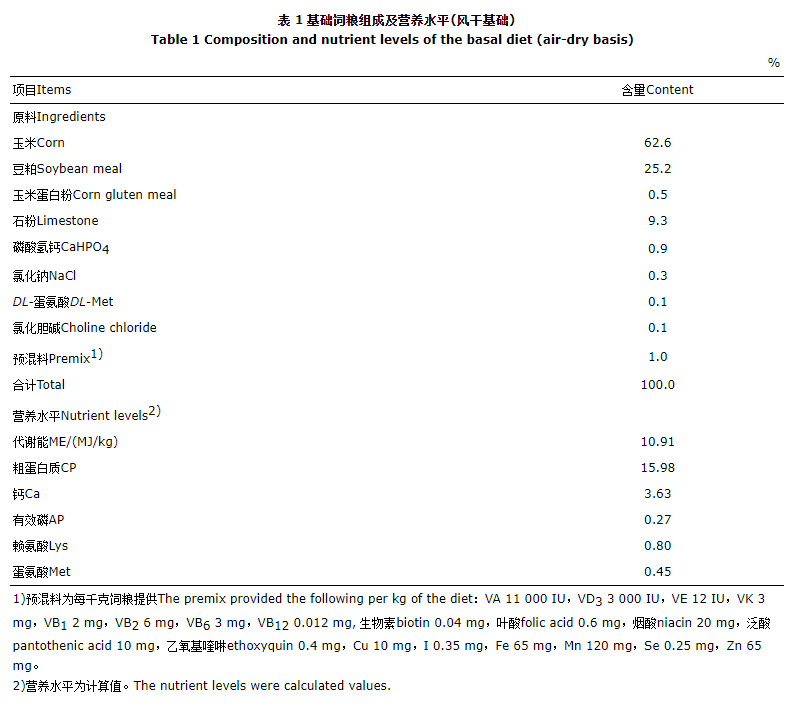
随机选取健康、体重相近的70周龄大午金凤蛋鸡60只,随机分为3组,每组4个重复,每个重复5只。对照组腹腔注射等量生理盐水,试验Ⅰ组腹腔注射20 mg/(kg·d)褪黑素,试验Ⅱ组腹腔注射50 mg/(kg·d)褪黑素。所有试验动物单笼饲养,控制温度条件为(23±2) ℃,相对湿度为(65±10)%,严格控制光照条件为16L:8D,试验期间自由采食,自由饮水。预试期7 d,正试期28 d。基础饲粮组成及营养水平见表1。
1.2 褪黑素注射程序
褪黑素购于美国Sigma-Aldrich公司(货号M5250),褪黑素先在10%无水乙醇充分溶解,再用生理盐水调整到试验浓度,并在每天的16:00进行注射,对照组的生理盐水无水乙醇浓度也调整为10%。试验鸡只在试验期进行称重,严格按照体重确定注射剂量。
1.3 样品采集与指标测定
1.3.1 样品采集
以个体为单位,每天记录蛋鸡的投料量与剩余料量、蛋重、产蛋数等,并以周为单位计算平均日采食量、产蛋率、料蛋比。每周每组随机取10个鸡蛋进行蛋品质测定,测定后蛋黄置于-80 ℃保存,用于蛋黄其他指标的测定。每周每组随机取10只鸡于试验第1、7、14、21、28天当天16:00进行采血,采集的血样3 000 r/min离心15 min,分离血清,-20 ℃保存,用于血清指标的测定。试验结束时,通过颈脱位方法对试验鸡只处死,完整取出卵巢,将不同等级卵泡分离并记录卵泡的数量,然后将卵巢基质取一部分于-80 ℃冻存,用于卵巢基质相关指标的测定。
1.3.2 生产性能指标

1.3.3 蛋品质指标
蛋形指数:利用蛋形指数测定仪(以色列NFN385)进行测定,测量鸡蛋最大纵径和横径,取纵径与横径之比为蛋形指数。
蛋壳厚度:采用游标卡尺进行测定,剥离蛋壳膜后,取钝端、锐端、中间部位3点进行测定,取平均值。
蛋壳强度:采用蛋壳强度分析仪(EFR-01,以色列)进行测定,将鸡蛋钝端向上,锐端向下放到蛋壳强度分析仪上,探头向下移动,当蛋壳出现第1道裂纹时即为蛋壳的强度。
蛋黄、蛋壳相对重:利用电子天平对蛋黄重、蛋壳重和蛋重进行测定后采用公式计算相对重。
![]()
蛋重、蛋白高度和哈氏单位:采用蛋品质分析仪(EA-01,以色列)进行测定,将鸡蛋轻轻打碎后,将其内容物轻轻放于盛载样品的平板上,采用激光技术进行测定。
1.3.4 血清指标测定
采用酶联免疫吸附试验(ELISA)法测定血清中褪黑素(MT)、活性氧(ROS)、免疫球蛋白(Ig)A、IgG、IgM含量,总抗氧化能力(T-AOC),超氧化物歧化酶(SOD)活性及促卵泡素(FSH)、促黄体素(LH)含量,试剂盒购自上海江莱生物科技有限公司,按照说明书进行操作。
1.3.5 蛋黄指标测定
将分离好的蛋黄离心称取1 g样品,加入9 mL预冷的磷酸盐缓冲液(PBS)于玻璃匀浆器充分混匀,最后将匀浆液于5 000 r/min离心10 min,取上清液检测。采用ELISA方法测定蛋黄中MT和ROS含量、T-AOC及SOD活性,试剂盒购自上海江莱生物科技有限公司,按照说明书进行操作。
1.3.6 卵巢指标测定
将卵巢基质倒入玻璃匀浆器后,加入预冷的PBS进行匀浆处理,上下转动研磨6~8 min,使组织充分匀浆化。采用ELISA方法测定卵巢中MT和ROS含量、T-AOC及SOD活性,试剂盒购自上海江莱生物科技有限公司,按照说明书进行操作。
1.3.7 发育卵泡数量观察与统计
将卵泡按直径进行分类:排卵前卵泡(PF):>10 mm,小黄卵泡(SYF):8~10 mm;大白卵泡(LWF):6~8 mm;中白卵泡(MWF):4~6 mm;小白卵泡(SWF):2~4 mm;初始卵泡(PE):< 2 mm[13]。
1.4 数据分析
采用SPSS 23.0软件中的one-way ANOVA程序对数据进行单因素方差分析,用Duncan氏法进行多重比较,试验数据均以“平均值±标准差”表示,P< 0.05表示差异显著,P< 0.01表示差异极显著。对于不符合正态分布的试验数据用中位数表示。
2 结果与分析
2.1 外源褪黑素对产蛋后期蛋鸡生产性能的影响
由表2可知,外源褪黑素并没有对第1~7天产蛋后期蛋鸡的生产性能产生显著的影响(P>0.05),在第8~14天时,试验Ⅰ组的产蛋率显著高于对照组和试验Ⅱ组(P<0.05),且料蛋比极显著低于对照组和试验Ⅱ组(P<0.01)。在第15~21天和第22~28天时,试验Ⅰ、Ⅱ组产蛋率极显著高于对照组(P<0.01),料蛋比极显著低于对照组(P<0.01)。

2.2外源褪黑素对产蛋后期蛋鸡发育卵泡数量的影响
由表3可知,试验Ⅰ、Ⅱ组排卵前卵泡、小黄卵泡和小白卵泡的数量都稍高于对照组,大白卵泡数量显著高于对照组(P< 0.05)。

2.3 外源褪黑素对产蛋后期蛋鸡蛋品质的影响
由表4可知,在第1~7天时,试验Ⅱ组蛋白高度显著高于对照组和试验I组(P<0.05);在第15~21天及第22~28天时,试验Ⅱ组蛋壳厚度和蛋壳强度稍高于对照组,但差异不显著(P>0.05)。


2.4 外源褪黑素对产蛋后期蛋鸡体内褪黑素含量的影响
由表5可知,在第7天时,与对照组相比,试验Ⅰ、Ⅱ组血清褪黑激素含量极显著高于对照组(P< 0.01),且试验Ⅰ组显著高于对照组(P< 0.05);在第21天时,试验Ⅱ组血清褪黑素含量极显著高于对照组和试验Ⅰ组(P< 0.01);在第28天时,试验Ⅰ、Ⅱ组血清褪黑素含量极显著高于对照组(P< 0.01)。在第14、21天时,试验Ⅱ组蛋黄褪黑素含量极显著高于试验Ⅰ组和对照组(P< 0.01);在第28天时,试验Ⅰ、Ⅱ组蛋黄褪黑素含量显著高于对照组(P< 0.05)。在第28天时,试验Ⅱ组卵巢褪黑素含量极显著高于对照组(P< 0.01),试验Ⅰ组显著高于对照组(P< 0.05)。

2.5 外源褪黑素对产蛋后期蛋鸡体内抗氧化指标的影响
由表6可知,在第14、21天时,试验Ⅱ组血清T-AOC极显著高于对照组(P< 0.01),且试验Ⅰ组显著高于对照组(P< 0.05);在第28天时,试验Ⅱ组血清T-AOC极显著高于试验Ⅰ组和对照组(P< 0.01)。在第14天时,试验Ⅱ组蛋黄T-AOC极显著高于试验I组和对照组(P< 0.01);在第21天时,试验Ⅱ组蛋黄T-AOC极显著高于试验I组(P< 0.01);在第28天时,试验Ⅱ组蛋黄T-AOC极显著高于对照组(P< 0.01),显著高于试验Ⅰ组(P< 0.05)。在第28天时,试验Ⅱ组卵巢T-AOC极显著高于对照组和试验Ⅰ组(P< 0.01)。

在第7、14和21天时,试验Ⅱ组血清SOD活性极显著高于试验Ⅰ组和对照组(P< 0.01);在第28天时,试验Ⅱ组的血清SOD活性极显著高于对照组(P< 0.01),试验Ⅰ组血清SOD活性显著高于对照组(P< 0.05)。在第21天时,试验Ⅱ组蛋黄SOD活性极显著高于试验Ⅰ组和对照组(P< 0.01);在第28天时,试验Ⅱ组蛋黄SOD活性极显著高于对照组(P< 0.01),试验I组显著高于对照组(P< 0.05)。在第28天时,试验Ⅱ组卵巢SOD活性极显著高于对照组(P< 0.01),且试验Ⅰ组显著高于对照组(P< 0.05)。
在第7天时,试验Ⅱ组血清ROS含量极显著低于对照组(P< 0.01),试验Ⅰ组显著低于对照组(P< 0.05);在第14和21天时,与对照组相比,试验Ⅱ组血清ROS含量显著降低(P< 0.05);在第28天时,试验Ⅱ组血清ROS含量极显著低于试验Ⅰ组和对照组(P< 0.01)。在第14天时,试验Ⅰ、Ⅱ组蛋黄ROS含量显著低于对照组(P< 0.05);在第21天时,试验Ⅰ、Ⅱ组蛋黄ROS含量极显著低于对照组(P< 0.01)。试验第28天时,试验Ⅰ、Ⅱ组卵巢ROS含量极显著低于对照组(P< 0.01),且试验Ⅱ组极显著低于试验Ⅰ组(P< 0.01)。
2.6 外源褪黑素对产蛋后期蛋鸡血清中免疫球蛋白含量的影响
由表7可知,血清中的IgA含量结果显示,第1天时各组之间没有显著差异(P>0.05);第7天时,试验Ⅰ、Ⅱ组显著高于对照组(P< 0.05);在第14天时,试验Ⅱ组极显著高于试验Ⅰ组和对照组(P< 0.01);在第21和28天时,试验Ⅰ、Ⅱ组极显著高于对照组(P< 0.01)。血清中的IgG含量结果显示,在第7天时,试验Ⅰ、Ⅱ组极显著高于对照组(P< 0.01);在第14天时,试验Ⅱ组极显著高于对照组(P< 0.01),显著高于试验Ⅰ组(P< 0.05);在第21和28天时,试验Ⅰ、Ⅱ组极显著高于对照组(P< 0.01)。血清中的IgM含量结果显示,在第21天时,试验Ⅱ组极显著高于对照组(P< 0.01),试验Ⅰ组显著高于对照组(P< 0.05),在第28天时,试验Ⅱ组显著高于对照组(P< 0.05)。

2.7外源褪黑素对产蛋后期蛋鸡血清中生殖激素含量的影响
由表8可知,在第14和21天时,试验组Ⅰ、Ⅱ组血清FSH含量极显著高于对照组(P< 0.01),在第28天时,试验Ⅱ组血清FSH含量极显著高于对照组(P< 0.01),显著高于试验Ⅰ组(P< 0.05)。血清LH含量的结果显示,在第21和28天时,试验组Ⅰ、Ⅱ组均极显著高于对照组(P< 0.01)。

3 讨论
3.1 外源褪黑素对产蛋后期蛋鸡生产性能及卵泡数量的影响
家禽卵巢以卵泡作为基本功能单位。卵泡的生长和发育是一个非常复杂的过程,具有严格有序的层次结构。通常只有1个小黄卵泡(直径< 8 mm)进入排卵前卵泡序列,最后排卵。其余的小黄卵泡被闭锁或吸收[14]。鸡的卵泡数量的多少决定着产蛋性能。蛋鸡卵巢卵泡数量随着年龄的增长而减少,且随年龄的增长,卵泡排卵时的体积不断增大[5]。研究发现,处于排卵时期的卵泡新陈代谢十分旺盛,此过程会产生大量的自由基,而高含量的褪黑素是使排卵过程顺利完成的重要保证[15]。产蛋后期蛋鸡体内的褪黑素含量降低,本研究结果表明,对70周龄产蛋后期蛋鸡腹腔注射褪黑素后可以显著提高大白卵泡的数量,且褪黑素组的产蛋率在添加第2周后显著升高。Jia[12]研究发现,在550日龄蛋鸡皮下埋入褪黑素(10 mg)时,产蛋率显著高于对照组。杨博等[16]研究发现,每天用3 mg褪黑素处理蛋鸭后其产蛋率显著高于对照组。褪黑激素-牛血清蛋白主动免疫促进了皖西白鹅的排卵,并提高了2年龄皖西白鹅的产蛋率[17]。这些结果都与本试验研究结果一致。褪黑素通过减少卵母细胞数量和质量的下降来延缓卵巢衰老[18]。这可能是由于褪黑素受体存在于鸡的卵巢[19]和卵巢颗粒细胞[20],褪黑素可以通过受体直接调节卵巢的功能。褪黑素可能发挥了其直接和间接抗氧化作用进而清除氧化应激产生的ROS,从而防止卵泡闭锁[21],褪黑素还可以调节颗粒细胞和卵泡内膜细胞中甾体生成酶的活性及其基因表达,调节性激素的生成,从而促进卵泡的生长发育,提高产蛋率,并且使产蛋后期产蛋率下降的趋势变得缓慢。
3.2 外源褪黑素对产蛋后期蛋鸡蛋品质的影响
本试验研究发现,外源补充褪黑素并没有对产蛋后期蛋鸡的蛋品质产生显著的影响,但是褪黑素组的蛋壳厚度和蛋壳强度都稍高于对照组。禽类松果体分泌的褪黑素可能通过介导降钙素、甲状旁腺素及雌激素分泌,节律性地调节体内钙代谢[22],从而影响蛋壳的形成。
3.3 外源褪黑素对产蛋后期蛋鸡抗氧化性能的影响
体内的自由基在正常生理条件下与抗氧化系统处于平衡状态。一旦平衡被打破,机体清除自由基的能力就会降低,导致ROS过度积累从而引起氧化应激。由ROS引起的氧化应激被认为是影响卵巢衰老的最直接因素[23]。机体的抗氧化酶主要是SOD。SOD活性是衡量机体抗氧化能力的重要指标之一[24]。SOD通过清除体内细胞中的自由基来保护细胞免受氧化应激的损伤。T-AOC反映生物体的总抗氧化能力。在本研究中,褪黑素组在注射第2周后显著增加了产蛋后期蛋鸡血清、蛋黄和卵巢的SOD活性和T-AOC。Ozturk等[25]研究发现,给予10 mg/kg褪黑素7 d后可显著提高大鼠的肝脏SOD活性。Kim等[26]报道了褪黑素(715 g/kg)处理14 d后大鼠血液中T-AOC和SOD活性增加。这些结果与本研究的结果一致。褪黑素被称为高效的自由基清除剂[21]。其自由基清除能力是维生素E的2倍、谷胱甘肽的4倍、甘露醇的14倍。在本研究中,与对照组相比,褪黑素组处理2周后血清、蛋黄的ROS含量显著降低。由于褪黑素独特的物理和化学特性,同时具备脂溶性和水溶性,使其能自由通过任何生理屏障,可以直接到达线粒体,因此与其他抗氧化剂相比更具有优势[27]。褪黑素可直接清除自由基[28]。而且褪黑素广泛分布于组织和细胞中[29],并通过其受体发挥广泛作用。本研究结果发现,褪黑素具有高效的ROS清除能力,并通过增强内源性抗氧化剂的产生间接抑制氧化应激。
3.4 外源褪黑素对产蛋后期蛋鸡免疫性能的影响
免疫性能是维持家禽健康的重要参数,研究发现鸽子的免疫性能在松果腺切除后减少,表明免疫功能受褪黑素调节[30]。在本研究中,外源补充褪黑素显著改善了血清中IgA、IgG、IgM含量。在第28天时,试验Ⅱ组的血清免疫球蛋白含量与对照组相比达到了极显著的水平。褪黑素的免疫调节作用可以通过与免疫细胞中的受体直接相互作用来介导。褪黑素受体存在于脾和淋巴组织中[31],褪黑激素与受体2-[125I]碘褪黑素结合位点反应,刺激免疫细胞产生免疫阿片类和淋巴因子,介导褪黑素的免疫调节功能。研究发现,外源补充褪黑素可以提高日本鹌鹑[32]和鸡[33]的细胞和体液免疫反应。褪黑素还可通过增加机体免疫器官的重量,并通过神经-内分泌-免疫网调控[34]。卢玉发[35]研究表明10 mg/kg褪黑素能够促进肉鸡主要免疫器官的发育,提高免疫器官指数。这与本研究结果一致,表明褪黑素直接作用于免疫系统从而提高机体的免疫性能。
3.5外源褪黑素对产蛋后期蛋鸡繁殖性能的影响
褪黑素通过下丘脑-垂体-性腺轴,在下丘脑水平上调节促性腺激素的分泌,进而影响生殖系统功能,并且与卵巢受体结合,直接调节性腺激素的合成和分泌[36]。本试验研究结果显示,对产蛋后期的蛋鸡进行外源补充褪黑素后,血清FSH含量在第2周,LH含量在第3周都开始显著升高。Jia[12]研究发现,在360日龄母鸡皮下埋入10 mg褪黑素后发现,血清FSH和LH含量显著升高,与本试验研究结果一致。高水平的褪黑素可以增加血清中LH和FSH的含量。而低含量的LH和FSH可以抑制排卵[37]。褪黑素及其受体在动物生殖过程的调节中起着至关重要的作用。因此,褪黑素的这些活动也可以帮助母鸡在产蛋高峰期后保持产蛋率。
3.6外源褪黑素对产蛋后期蛋鸡体内褪黑素含量的影响
内源褪黑素主要由松果体合成、分泌,是脂溶性的,因此可以通过松果体细胞内的细胞膜进入到血液中,分解代谢主要是在肝脏和脑中进行,代谢产物则随尿液排出[38]。褪黑素只有与特异的受体结合才能发挥生物学作用。已有研究证实,褪黑素受体存在于鸡的卵巢[19]、鸡卵巢颗粒细胞[20]及鸡脑、肾脏、脾脏、肺[31]。蛋鸡随周龄增加体内褪黑素分泌水平变低,而且下丘脑-垂体-性腺轴对生殖激素的敏感性变弱,外源注射褪黑素处理后,褪黑素可能与相应受体结合从而提高了蛋鸡血液、蛋黄和卵巢基质中的褪黑素含量,这表明外源性注射褪黑激素显著增加了蛋鸡体内的褪黑素含量。
4 结论
① 50 mg/(kg·d)外源褪黑素处理2周后可以显著提高产蛋后期蛋鸡的产蛋率及大白卵泡的数量。
② 50 mg/(kg·d)外源褪黑素处理2周后显著提高了血清和蛋黄中的褪黑素含量、SOD活性及T-AOC,显著降低了ROS含量。
③ 50 mg/(kg·d)外源褪黑素处理2周后显著提高了血清中免疫球蛋白含量及生殖激素FSH和LH含量。

郝二英,黄晨轩,孙浩政,王德贺,周荣艳,黄仁录,陈辉.外源褪黑素对产蛋后期蛋鸡生产性能、血清指标及体内褪黑素含量的影响[J].动物营养学报, 2020, 32(5):2126-2137.
HAO Erying, HUANG Chenxuan, SUN Haozheng, WANG Dehe, ZHOU Rongyan, HUANG Renlu, CHEN Hui. Effects of Exogenous Melatonin on Performance, Serum Indexes and Melatonin Content of Laying Hens during Later Laying Period[J]. Chinese Journal of Animal Nutrition, 2020, 32(5):2126-2137.
参考文献
[1] ROLAND D A. Factors influencing shell quality of aging hens[J]. Poultry Science, 1979, 58(4):774-777. DOI:10.3382/ps.0580774
[2] WILLIAMS K C. Some factors affecting albumen quality with particular reference to Haugh unit score[J]. World's Poultry Science Journal, 1992, 48(1):5-16. DOI:10.1079/WPS19920002
[3] AL-BATSHAN H A, SCHEIDELER S E, BLACK B L, et al. Duodenal calcium uptake, femur ash, and eggshell quality decline with age and increase following molt[J]. Poultry Science, 1994, 73(10):1590-1596. DOI:10.3382/ps.0731590
[4] GROSSMAN M, GOSSMAN T N, KOOPS W J. A model for persistency of egg production[J]. Poultry Science, 2000, 79(12):1715-1724. DOI:10.1093/ps/79.12.1715
[5] ZAKARIA A H, MIYAKI T, IMAI K. The effect of aging on the ovarian follicular growth in laying hens[J]. Poultry Science, 1983, 62(4):670-674. DOI:10.3382/ps.0620670
[6] LERNER A B, CASE J D, TAKAHASHI Y, et al. Isolation of melatonin, the pineal gland factor that lightens melanocytes[J]. Journal of the American Chemical Society, 1958, 80(10):2587. DOI:10.1021/ja01543a060
[7] REITER R J. Pineal melatonin:cell biology of its synthesis and of its physiological interactions[J]. Endocrine Reviews, 1991, 12(2):151-180.
[8] ZHOU W, ZHANG X, ZHU C L, et al. Melatonin receptor agonists as the "perioceutics" agents for periodontal disease through modulation of Porphyromonas gingivalis virulence and inflammatory response[J]. PLoS One, 2016, 11(11):e0166442. DOI:10.1371/journal.pone.0166442
[9] SÖDERQUIST F, JANSON E T, RASMUSSON A J, et al. Melatonin immunoreactivity in malignant small intestinal neuroendocrine tumours[J]. PLoS One, 2016, 11(10):e0164354. DOI:10.1371/journal.pone.0164354
[10] MEHAISEN G M K, SAEED A M, GAD A, et al. Antioxidant capacity of melatonin on preimplantation development of fresh and vitrified rabbit embryos:morphological and molecular aspects[J]. PLoS One, 2015, 10(10):e0139814. DOI:10.1371/journal.pone.0139814
[11] REITER R J. Interactions of the pineal hormone melatonin with oxygen-centered free radicals:a brief review[J]. Brazilian Journal of Medical & Biological Research, 1993, 26(11):1141-1155.
[12] JIA Y X, YANG M H, ZHU K F, et al. Melatonin implantation improved the egg-laying rate and quality in hens past their peak egg-laying age[J]. Scientific Reports, 2016, 6:39799. DOI:10.1038/srep39799
[13] JOHNSON A L. Ovarian follicle selection and granulosa cell differentiation[J]. Poultry Science, 2015, 94(4):781-785. DOI:10.3382/ps/peu008
[14] GILBERT A B, PERRY M M, WADDINGTON D, et al. Role of atresia in establishing the follicular hierarchy in the ovary of the domestic hen (Gallus domesticus)[J]. J Reprod Fertil, 1983, 69(1):221-227.
[15] REITER R J, ROSALES-CORRAL S A, MANCHESTER L C, et al. Peripheral reproductive organ health and melatonin:ready for prime time[J]. International Journal of Molecular Sciences, 2013, 14(4):7231-7272. DOI:10.3390/ijms14047231
[16] 杨博,江丹莉,钱隆,等.饲喂外源性褪黑素对蛋鸭产蛋性能及生殖激素的影响[J].仲恺农业工程学院学报, 2018, 31(2):46-49. DOI:10.3969/j.issn.1674-5663.2018.02.010
[17] 凌明亮,黄仁术.褪黑激素-牛血清蛋白主动免疫对皖西白鹅性腺表征的影响[J].中国兽医学报, 2007, 27(1):84-87. DOI:10.3969/j.issn.1005-4545.2007.01.021
[18] TAMURA H, KAWAMOTO M, SATO S, et al. Long-term melatonin treatment delays ovarian aging[J]. Journal of Pineal Research, 2017, 62(2):e12381. DOI:10.1111/jpi.12381
[19] AYRE E A, YUAN H, PANG S F. The identification of 125I-labelled iodomelatonin-binding sites in the testes and ovaries of the chicken (Gallus domesticus)[J]. Journal of Endocrinology, 1992, 133(1):5-11.
[20] SUNDARESAN N R, LEO M D M, SUBRAMANI J, ET al. Expression analysis of melatonin receptor subtypes in the ovary of domestic chicken[J]. Veterinary Research Communications, 2009, 33(1):49-56. DOI:10.1007/s11259-008-9071-9
[21] TAMURA H, TAKASAKI A, TAKETANI T, et al. Melatonin as a free radical scavenger in the ovarian follicle[J]. Endocrine Journal, 2013, 60(1):1-13.
[22] LADIZESKY M G, BOGGIO V, ALBORNOZ L E, et al. Melatonin increases oestradiol-induced bone formation in ovariectomized rats[J]. Journal of Pineal Research, 2010, 34(2):143-151.
[23] GRØNDAHL M L, ANDERSEN C Y, BOGSTAD J, et al. Gene expression profiles of single human mature oocytes in relation to age[J]. Human Reproduction, 2010, 25(4):957-968. DOI:10.1093/humrep/deq014
[24] RAGEL B T, BROWD S R, SCHMIDT R H. Surgical shunt infection:significant reduction when using intraventricular and systemic antibiotic agents[J]. Journal of Neurosurgery, 2006, 105(2):242-247. DOI:10.3171/jns.2006.105.2.242
[25] ÖZTVRK G, COŞKUN S, ERBAŞ D, et al. The effect of melatonin on liver superoxide dismutase activity, serum nitrate and thyroid hormone levels[J]. The Japanese Journal of Physiology, 2000, 50(1):149-153.
[26] KIM Y H, LEE S H, MUN K C. Effect of melatonin on antioxidant status in the plasma of cyclosporine-treated rats[J]. Transplantation Proceedings, 2002, 34(7):2652-2653. DOI:10.1016/S0041-1345(02)03462-0
[27] TANABE M, TAMURA H, TAKETANI T, et al. Melatonin protects the integrity of granulosa cells by reducing oxidative stress in nuclei, mitochondria, and plasma membranes in mice[J]. Journal of Reproduction and Development, 2015, 61(1):35-41.
[28] REITER R J, MAYO J C, TAN D X, et al. Melatonin as an antioxidant:under promises but over delivers[J]. Journal of Pineal Research, 2016, 61(3):253-278. DOI:10.1111/jpi.12360
[29] MEREDITH S, JACKSON K, DUDENHOEFFER G, et al. Long-term supplementation with melatonin delays reproductive senescence in rats, without an effect on number of primordial follicles[J]. Experimental Gerontology, 2000, 35(3):343-352. DOI:10.1016/S0531-5565(00)00092-9
[30] RODRÍGUEZ A B, LEA R W. Effect of pinealectomy upon the nonspecific immune response of the ring-dove (Streptopelia risoria)[J]. Journal of Pineal Research, 2010, 16(3):159-166. DOI:10.1111/j.1600-079X.1994.tb00096.x
[31] PANG C S, TANG P L, PANG S F, et al. Comparison of the pharmacological characteristics of 2-[125Ⅰ]iodomelatonin binding sites in the lung, spleen, brain and kidney of chicken[J]. Biological Signals, 1995, 4(6):311-324. DOI:10.1159/000109465
[32] MOORE C B, SIOPES T D. Effects of lighting conditions and melatonin supplementation on the cellular and humoral immune responses in Japanese quail Coturnix coturnix japonica[J]. General and Comparative Endocrinology, 2000, 119(1):95-104.
[33] MOORE C B, SIOPES T D. Effect of melatonin supplementation on the ontogeny of immunity in the large white turkey poult[J]. Poultry Science, 2002, 81(12):1898-1903. DOI:10.1093/ps/81.12.1898
[34] CALVO J R, GONZÁLEZ-YANES C, MALDONADO M D.The role of melatonin in the cells of the innate immunity:a review[J].Journal of Pineal Research, 55(2):103-120.
[35] 卢玉发,廖清华.褪黑素对肉鸡生长性能及免疫功能的影响[J].饲料工业, 2008, 29(13):37-39. DOI:10.3969/j.issn.1001-991X.2008.13.011
[36] 茆达干,杨利国,吴结革.褪黑激素对动物生殖的作用及其调控[J].草食家畜, 2001(3):5-8,24. DOI:10.3969/j.issn.1003-6377.2001.03.002
[37] ODELL W D, SWERDLOFF R S. Progestogen-induced luteinizing and follicle-stimulating hormone surge in postmenopausal women:a simulated ovulatory peak[J]. Proceedings of the National Academy of Sciences of the United States of America, 1968, 61(2):529-536. DOI:10.1073/pnas.61.2.529
[38] 杨振军,杨松鹤,陈志宏.有关褪黑素的研究进展[J].承德医学院学报, 2004, 21(1):74-77. DOI:10.3969/j.issn.1004-6879.2004.01.049
 会员投稿
会员投稿 手机版
手机版 | 营养频道
| 营养频道














